
Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
Epstein-Barr-virusprotein øger kræftgenaktiviteten i HPV-positive livmoderhalsceller
Sidst revideret: 23.08.2025
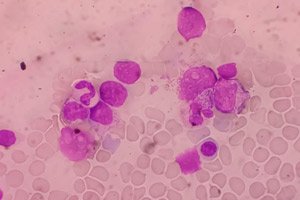 ">
">Forskere har vist, at Epstein-Barr-virus-nuklearantigenet EBNA1 er i stand til at forstærke ekspressionen af to cellulære gener forbundet med tumorprogression på én gang - Derlin1 (DERL1) og PSMD10 ( gankyrin ) - i HeLa-modellen af livmoderhalskræft. I eksperimentet blev tre grupper af celler sammenlignet: med EBNA1-ekspression, med et "tomt" kontrolplasmid og uden transfektion. Efter isolering af RNA blev mRNA-niveauet målt ved RT-qPCR, og forskellene blev vurderet (Mann-Whitney, p < 0,05). Resultat: På baggrund af EBNA1 steg DERL1 cirka 3 gange (p ≈ 0,028), PSMD10 - cirka 2 gange (p ≈ 0,02-0,03); ændringer i ZEB1 og CNN3 var statistisk insignifikante. Forfatterne foreslog, at en sådan transkriptionel 'vridning' kan understøtte tumorcelleoverlevelse og accelerere progression af livmoderhalskræft, især i forbindelse med mulig HPV+EBV-coinfektion.
Baggrund for undersøgelsen
Livmoderhalskræft er næsten altid forbundet med persistensen af højt onkogene HPV-typer, men stigende evidens tyder på, at co-infektioner spiller en rolle i at accelerere malignitet og progression. Epstein-Barr-virus (EBV) findes ofte i livmoderhalsvæv i forbindelse med HPV; meta-reviews og case-serier har forbundet denne "duet" med højere grader af dysplasi og ugunstige molekylære træk. Det foreslås, at EBV kan forstærke HPV-transformationssignaler, øge cellulær resistens over for apoptose og omdanne tumorens mikromiljø.
Det vigtigste EBV-latensprotein, EBNA1, findes i næsten alle EBV-associerede tumorer. Det opretholder antallet af episomkopier, regulerer virale promotorer og er i stand til at påvirke cellulær gentranskription og derved finjustere værtens ekspressionsnetværk. Disse egenskaber gør EBNA1 til en sandsynlig cofaktor i kræftudvikling og et kandidatmål for interventioner i EBV-positive epiteltumorer.
Gener forbundet med proteinkvalitetskontrol og -nedbrydning betragtes som potentielle "knudepunkter" for en sådan effekt. Derlin1 (DERL1) er en komponent af ERAD (ER removal of misfolded proteins)-signalvejen, som, når den er hyperaktiveret, understøtter overlevelsen af stressede kræftceller; PSMD10 (gankyrin) er en regulatorisk underenhed af proteasomet, der er kendt for at undertrykke p53/RB-signalvejen og øge proliferation. Begge gener er gentagne gange blevet beskrevet som pro-onkogene i forskellige modeller og er derfor af interesse som læsere af effekten af EBV på det cellulære miljø.
På denne baggrund tester et nyt studie i Genes & Cancer, om EBNA1 direkte kan "tune" ekspressionen af DERL1 og PSMD10 i livmoderhalskræftceller (HeLa-model) og derved bidrage til overlevelses-/resistensfænotypen. Forfatterne evaluerer mRNA-niveauerne af målgenerne sammenlignet med kontrolgruppen og diskuterer det resulterende signalmønster som en mulig molekylær signatur af EBV under samtidig infektion med HPV.
Hvorfor er dette vigtigt?
HPV er den primære ætiologiske faktor for livmoderhalskræft, men yderligere "cofaktorer" er ofte nødvendige for malign transformation. EBV er kendt som en oncovirus i epiteliale og lymfoide tumorer og findes ofte i livmoderhalsvæv sammen med HPV. Ved at vise, at et af de vigtigste latente proteiner i EBV direkte ændrer ekspressionen af gener involveret i ER-stress (DERL1) og regulering af proteasom/p53-RB-signalvejen (gankyrin, PSMD10), rejser vores arbejde et praktisk spørgsmål: Kan EBV øge cervikale cellers resistens over for apoptose og behandling, hvilket gør tumoren mere "levedygtig"?
Hvem er det præcis, EBNA1 "rører"?
- DERL1 (Derlin1) er et membranprotein i det endoplasmatiske reticulum, en deltager i systemet til fjernelse af misfoldede proteiner (ERAD); dets overekspression er forbundet med cellevækst/migration og resistens over for apoptose.
- PSMD10 (gankyrin) er en regulatorisk underenhed af 26S-proteasomet; den påvirker p53 og RB1 negativt via MDM2/CDK4-aksen og understøtter tumorproliferation og -overlevelse.
- ZEB1 er en transkriptionel regulator af epitelial-mesenkymal overgang (EMT); øget ekspression ledsager ofte invasion og lægemiddelresistens.
- CNN3 - aktin-relateret calponin-3; associeret med migration/metastase i nogle solide tumorer.
Sådan læser du disse data uden unødvendig hype
Dette er en in vitro-model på én cellelinje (HeLa), målingerne er kun på mRNA-niveau uden bekræftelse ved proteintests (Western, immunhistokemi), funktionelle konsekvenser (proliferation, invasion, apoptose) blev ikke testet. Der er ingen sammenligning med normalt cervikalt epitel og med andre HPV-statusser, hvilket betyder, at resultaternes overførbarhed til klinikken er begrænset. Dette gør et klart "signal" for to gener endnu mere værdifuldt: det skitserer det molekylære spor af EBNA1, hvilket er værd at undersøge i co-infektionsmodeller af HPV/EBV, på primært materiale og i dyreforsøg.
Hvad dette kan betyde videre - praktiske implikationer og hypoteser
- Biomarkører for samtidig infektion: Kombinationen af HPV-profil med DERL1/PSMD10-ekspression og EBV-markører kan hjælpe med at identificere risikogrupper og forudsige resistens over for behandling.
- Terapeutiske indgangspunkter: Hvis EBNA1 konsekvent opregulerer DERL1/PSMD10, er det logisk at teste inhibitorer af ER stress/ERAD-signalvejen og modifikatorer af proteasom/p53-MDM2-aksen i en EBV-positiv kontekst.
- Diagnostisk stratificering. I kliniske serier af livmoderhalskræft er det værd at korrelere EBV-status med behandlingsresultater og DERL1/PSMD10-ekspression for at forstå, hvem der har et yderligere "viralt bidrag" til aggressivitet.
Forfatterne anerkender begrænsningerne - og det er et plus
- Én HeLa-linje; ingen HPV-positive/negative linjepaneler.
- Intet protein og funktionel bekræftelse (kun RT-qPCR).
- Undersøgelsen er associativ: mekanismen for direkte regulering af EBNA1-promotorer for disse gener er ikke blevet vist, ligesom virkningernes afhængighed af dosis/tid.
- Der er ikke udført validering på kliniske cervikale prøver.
Konklusion
Arbejdet tilføjer på en elegant måde en ny byggesten til vores forståelse af muligt HPV-EBV-samarbejde i livmoderhalskræft: det latente protein EBNA1 er i stand til at ændre ekspressionen af gener, der understøtter tumorcelleoverlevelse og -proliferation. Kliniske implikationer er stadig langt ude i fremtiden, men DERL1 og PSMD10 ser ud til at være rimelige kandidater til indikatorer og mål i den EBV-positive kontekst – forudsat at resultaterne bekræftes på proteinniveau, funktion og i reelt tumorvæv.
Kilde: Alipour AH, Hashemi SMA, Gharahkhani F., Katanchi A., Farhadi A., Sarvari J. Epstein-Barr virus nuklear antigen 1 opregulerer Derlin1 og PSMD10 ekspression i HeLa celler. Gener & Cancer (accepteret 24. juli 2025; offentliggjort 6. august 2025). https://doi.org/10.18632/genesandcancer.242
