
Alt iLive-indhold gennemgås medie eller kontrolleres for at sikre så meget faktuel nøjagtighed som muligt.
Vi har strenge sourcing retningslinjer og kun link til velrenommerede medie websteder, akademiske forskningsinstitutioner og, når det er muligt, medicinsk peer reviewed undersøgelser. Bemærk at tallene inden for parentes ([1], [2] osv.) Er klikbare links til disse undersøgelser.
Hvis du mener, at noget af vores indhold er unøjagtigt, forældet eller på anden måde tvivlsomt, skal du vælge det og trykke på Ctrl + Enter.
Hypofysemikroadenom: årsager, symptomer, fare, prognose
Medicinsk ekspert af artiklen
Sidst revideret: 12.07.2025
Godartede neoplasmer, der opstår i de endokrine kirtler, kaldes adenomer, og et mikroadenom i hypofysen er en lille tumor i dens forreste lap, som producerer en række vigtige hormoner.
Epidemiologi
Forekomsten af hypofysetumorer anslås at være 10-23%, og hypofyseadenomer, som kan have forskellige former og størrelser, er de mest almindelige (16%).[ 1 ]
Op til 20-25 % af befolkningen kan have små hypofysetumorer, mikroadenomer, uden at vide det, og sådanne tumorer opdages tilfældigt under hjernebilleddannelse i omkring halvdelen af tilfældene.
Prolaktinsekreterende mikroadenomer tegner sig for 45-75% af sådanne tumorer; ACTH-producerende formationer tegner sig for højst 14% af tilfældene, og hyppigheden af STH-producerende mikroadenomer overstiger ikke 2%.
Mikroadenom i hypofysen hos børn og unge påvises i 10,7-28% af tilfældene, og mindst halvdelen af dem er hormonelt inaktive. [ 2 ]
Årsager Hypofyse-mikroadenomer
Eksperter kender ikke de nøjagtige årsager til forekomsten af mikroadenom i hypofysen, en endokrin kirtel i hjernen, hvis celler producerer:
- kortikotropin eller ACTH – adrenokortikotropt hormon, som forårsager udskillelse af steroidhormoner fra binyrebarken;
- væksthormon STH – somatotropisk hormon;
- gonadotropinerne FSH – follikelstimulerende hormon og LH – luteiniserende hormon, som bestemmer produktionen af kvindelige kønshormoner i æggestokkene og mandlige kønshormoner i testiklerne;
- laktogen hormonprolaktin (PRL);
- thyrotropin eller thyreoideastimulerende hormon (TSH), som stimulerer syntesen af hormoner i skjoldbruskkirtlen.
Det menes, at udviklingen af disse neoplasmer kan være forårsaget af traumatisk hjerneskade; utilstrækkelig blodforsyning til hypofysen; cerebrale infektioner eller eksponering for toksiner (som forårsager ødem og intrakraniel hypertension).
Risikofaktorer
Det er kendt, at hypofyseadenomer og mikroadenomer forekommer oftere i tilfælde af MEN 1-syndrom - multipel endokrin adenomatose type 1, som er arvelig i familien. Der er således genetisk bestemte risikofaktorer forbundet med visse ændringer i DNA. [ 3 ]
Multipel endokrin neoplasi type 4 (MEN4): MEN 4 har en mutation i det cyclin-afhængige kinasehæmmer 1 B (CDKN1B)-gen, som er karakteriseret ved hypofysetumorer, hyperparathyroidisme, neuroendokrine tumorer i testiklerne og livmoderhalsen.[ 4 ]
Carney-kompleks (CNC): I Carney-komplekset er der en kimlinjemutation i tumorsuppressorgenet PRKAR1A, der fører til primær pigmenteret nodulær adrenokortikal sygdom (PPNAD), testikulære tumorer, skjoldbruskkirtelknuder, pletvis hyperpigmentering af huden og akromegali.[ 5 ]
Den kliniske form af familiære isolerede hypofyseadenomer (FIPA) er karakteriseret ved genetiske defekter i arylcarbonhydridreceptor-interagerende protein (AIP)-genet i cirka 15 % af alle relaterede og 50 % af homogene somatotropinfamilier.[ 6 ]
Familiære isolerede hypofyseadenomer (FIPA): En mutation i arylcarbonhydridreceptor-interagerende protein (AIP) påvises i ungdomsårene eller tidlig voksenalder i cirka 15 % af alle FIPA-tilfælde. Disse tumorer er typisk aggressive og udskiller oftest væksthormon, hvilket forårsager akromegali.[ 7 ]
Muligheden for, at denne type tumor opstår som følge af funktionelle forstyrrelser hos andre endokrine kirtler og cerebrale strukturer, især ændringer i hypothalamus' vaskulære system, som inden for det neuroendokrine hypothalamus-hypofysesystem regulerer funktionen af hypofysen og dens forlap, adenohypofysen, med dens frigivende hormoner, er ikke udelukket.
Patogenese
Ifølge sin histologi er hypofyseadenom en godartet tumor; afhængigt af størrelsen er disse neoplasmer opdelt i mikroadenomer (op til 10 mm i størrelse på det bredeste punkt), makroadenomer (10-40 mm) og kæmpeadenomer (40 mm eller mere).
Mens man studerer patogenesen af tumordannelse i hypofysen, har det endnu ikke været muligt at bestemme mekanismerne for hyperplastisk transformation af celler i dens forreste lob til en tumor.
Eksperter mener, at en af de mest overbevisende versioner er en forbindelse med dereguleringen af metabolismen af neurotransmitteren og hormonet dopamin (som er den primære hæmmer af prolaktinsekretion) og/eller en forstyrrelse af funktionerne af transmembrane dopaminreceptorer i hypofyseceller, der udskiller PRL (laktotrofer).
De fleste hypofysemikroadenomer er sporadiske, men nogle forekommer som en del af genetisk bestemte neuroendokrine syndromer såsom MEN 1, McCune-Albright syndrom, Werners syndrom og Carney syndrom (eller Carney-kompleks). Sidstnævnte er forbundet med en øget risiko for at udvikle godartede tumorer i hormonelle (endokrine) kirtler, herunder hypofysen, binyrerne, skjoldbruskkirtlen, æggestokkene og testiklerne.
Symptomer Hypofyse-mikroadenomer
Et hypofyse-mikroadenom viser muligvis ingen symptomer i meget lang tid. Symptomerne varierer afhængigt af placeringen og opstår normalt som følge af endokrin dysfunktion. Dette er det mest almindelige fund i tilfælde af hormonel ubalance forbundet med overdreven produktion af et eller flere hormoner. I de fleste tilfælde er dette, baseret på placering, et mikroadenom i den forreste hypofyse.
Der findes forskellige typer hypofysemikroadenomer baseret på deres hormonelle aktivitet. Den mest almindelige type anses derfor for at være et ikke-fungerende adenom – et hormonelt inaktivt hypofysemikroadenom, som – indtil det når en vis størrelse – ikke giver nogen symptomer. Men et voksende hormonelt inaktivt hypofysemikroadenom kan komprimere nærliggende hjernestrukturer eller kranienerver, så et hypofysemikroadenom og hovedpine i frontal- og temporalregionerne kan kombineres, [ 8 ] og synsproblemer er også mulige. [ 9 ] Men som forskere hævder, er ikke-fungerende (hormonelt inaktive) hypofysetumorer i 96,5% af tilfældene makroadenomer. [ 10 ]
Hormonelt aktivt mikroadenom i hypofysen (dens forlap) med øget sekretion af hormonet prolaktin kan også forekomme - prolaktinom i hypofysen. Øget produktion af PRL af laktotrope celler i adenohypofysen defineres som hyperprolaktinæmi i hypofysemikroadenom.
Hvordan manifesterer et sådant hypofyse-mikroadenom sig hos kvinder? Patologisk høje niveauer af dette hormon hæmmer produktionen af østrogener, og de første tegn manifesterer sig ved menstruationscyklusforstyrrelser - med fravær af menstruation (amenoré) og/eller deres ovulatoriske fase. Som følge heraf udvikles vedvarende galaktoré-amenoré-syndrom, og evnen til at blive gravid og blive gravid går tabt.
Prolaktinsekreterende hypofysemikroadenom hos mænd kan føre til hyperprolaktinæmisk hypogonadisme med nedsat libido, erektil dysfunktion, forstørrede bryster (gynækomasti) og nedsat ansigts- og kropsbehåring.
Aktivt mikroødemesekreterende kortikotropin (ACTH) fører til et overskud af steroidhormoner (glukokortikoider) produceret af binyrebarken, hvilket kan forårsage Itsenko-Cushings sygdom i hypofysen.
Hos børn kan et sådant mikroadenom manifestere sig med symptomer på hyperkorticisme (Cushings syndrom), herunder hovedpine, generel svaghed, overskydende fedtvævsaflejring på kroppen, nedsat knoglemineraltæthed og muskelstyrke, strimmellignende atrofi af huden (i form af lilla striber) osv.
Med et aktivt somatotropinproducerende mikroadenom stiger niveauet af STH i kroppen. I barndommen stimulerer dets overdrevne anabolske effekt væksten af næsten alle knogler i kroppen og kan føre til gigantisme; hos voksne kan akromegali udvikle sig med øget vækst af ansigtsknoglerne (forårsager forvrængning af udseende) og brusk i ekstremiteternes led (hvilket fører til en krænkelse af deres proportioner og fortykkelse af fingrene), med ledsmerter, overdreven svedtendens og talgproduktion samt nedsat glukosetolerance.
Meget sjældent (i 1-1,5% af tilfældene) er der et mikroadenom i hypofysen, der producerer thyrotropin, og da dette hormon har en stimulerende effekt på skjoldbruskkirtlen, har patienter kliniske tegn på hypofysehypertyreose i form af sinus takykardi og atrieflimren i hjertet, forhøjet blodtryk, nedsat kropsvægt (med øget appetit) samt øget nervøs excitabilitet og irritabilitet.
Det såkaldte intrasellære mikroadenom i hypofysen, synonymt - endosellært mikroadenom i hypofysen, er ligesom hele hypofysen lokaliseret i sella turcica - inde i den anatomiske sadelformede fordybning i sphenoidbenet ved kraniebunden. Samtidig er hypofysen placeret i bunden af denne fordybning - i hypofysefossa (intrasellær region). Og hele forskellen i ordene er, at "inde" på latin er intra, og på græsk - endom.
Men et hypofyse-mikroadenom med suprasellær vækst betyder, at neoplasmen vokser opad fra bunden af hypofysefossaen.
Cystisk mikroadenom i hypofysen har en lukket sæklignende struktur og er en asymptomatisk formation.
Mikroadenom i hypofysen med blødning kan være resultatet af apopleksi eller hæmoragisk infarkt forbundet med forstørrelse af kirtlen og skade på sinusformede kapillærer i parenkymet i dens forreste lob, neurohemale synapser og/eller portalkar.
Mikroadenom i hypofysen og graviditet
Som allerede nævnt er kvinder med prolaktinproducerende hypofysemikroadenom normalt infertile på grund af østrogenmangel og undertrykkelse af den pulserende sekretion af GnRH (gonadotropinfrigivende hormon). For at blive gravid skal prolaktinniveauet normaliseres, ellers forekommer undfangelsen ikke, eller graviditeten afbrydes helt i begyndelsen.
- Er det muligt at føde med et hypofyse-mikroadenom?
Hos kvinder med klinisk fungerende mikroadenomer, der behandles med dopaminagonister (Cabergolin eller Dostinex), kan prolaktinniveauerne normaliseres, og menstruationscyklusser og fertilitet kan genoprettes.
Er amning mulig med hypofyse-mikroadenom?
I postpartumperioden er amning tilladt, hvis der ikke er symptomer på tumoren, men det er nødvendigt at overvåge dens størrelse (ved hjælp af magnetisk resonansbilleddannelse af hjernen). Og hvis tumoren vokser, stoppes amningen.
- Mikroadenom i hypofysen og IVF
Behandling af hyperprolaktinæmi er nødvendig i forbindelse med IVF, og proceduren kan påbegyndes, hvis normale prolaktinniveauer har været stabile i 12 måneder, og der ikke er nogen abnormiteter i serumniveauerne af andre hypofysehormoner.
Komplikationer og konsekvenser
Hvad er farligt ved hypofyse-mikroadenom? Selvom denne tumor er godartet, kan dens tilstedeværelse forårsage komplikationer og have konsekvenser, især:
- føre til dysfunktion af hypothalamus-hypofyse-binyresystemet med udviklingen af Itsenko-Cushings sygdom;
- forstyrre hormonreguleringen af menstruationscyklussen hos kvinder og føre til erektil dysfunktion hos mænd;
- forårsage væksthæmning og hypofysedværgvækst (hypopituitarisme) hos børn;
- fremprovokere udviklingen af osteoporose.
Når en voksende tumor komprimerer synsnervefibrene i det område, hvor de krydses (som hos 80% af mennesker er placeret direkte over hypofysen), sker der en forstyrrelse i øjets mobilitet (oftalmoplegi) og en gradvis forværring af det perifere syn. Mikroadenomer er dog normalt for små til at udøve et sådant tryk.
Kan et hypofyse-mikroadenom forsvinde? Det kan ikke forsvinde, men over tid kan en hormonelt inaktiv tumor hos børn mindskes betydeligt. Men hos omkring 10% af patienterne kan mikroadenomer øges i størrelse.
Diagnosticering Hypofyse-mikroadenomer
For at diagnosticere et hypofyse-mikroadenom kræves en fuldstændig patienthistorie og laboratorietests: blodprøver for hormonniveauer (produceret af hypofysen), inklusive en radioimmunoassay af blodserum for prolaktinniveauer.
Hvis prolaktin er normalt med et hypofyse-mikroadenom, er denne tumor hormonelt inaktiv. Men hvis der er symptomer på prolaktinom, kan et sådant falsk negativt resultat enten være resultatet af en laboratorietestfejl, eller at patienten har udviklet et makroadenom, der komprimerer hypofysen.
Derudover kan yderligere tests være nødvendige, for eksempel for niveauet af skjoldbruskkirtelhormoner (T3 og T4), immunoglobuliner, interleukin-6 i blodserumet.
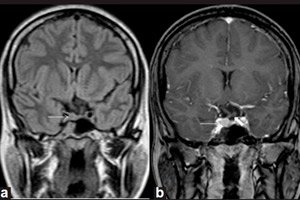
Mikroadenom kan kun detekteres ved instrumentel diagnostik med magnetisk resonansbilleddannelse (MRI) af hjernen. Og MR til mikroadenom betragtes som standarden for visualisering, med en følsomhed på 90% af MR med kontrastforstærkning.
Tegn på hypofyse-mikroadenom ved MR-scanning omfatter: kirtelvolumen på siden af mikroadenomet; en forøgelse af sella turcicas størrelse; udtynding og ændringer i funduskonturen (nederste væg); lateral afvigelse af hypofysens infundibulum; isointensitet af det afrundede område sammenlignet med grå substans på T1- og T2-vægtede billeder; let hyperintensitet på T2-vægtede billeder. [ 11 ]
Differential diagnose
Differentialdiagnostik udføres med kraniofaryngeom, granulær celletumor (koristom) i hypofysen, Rathkes pouchcyste, dermoiddannelse, betændelse i hypofysen - autoimmun eller lymfocytisk hypofysitis, fæokromocytom, skjoldbruskkirtelsygdomme osv.
Hos kvinder med en anovulatorisk cyklus er der differentieret mellem hypofysemikroadenom og polycystisk ovariesyndrom, da 75-90% af tilfældene med manglende ægløsning er en konsekvens af polycystisk ovariesyndrom.
Hvem skal kontakte?
Behandling Hypofyse-mikroadenomer
I tilfælde af adenomer og mikroadenomer i hypofysen kan behandlingen være medicinsk og kirurgisk. Samtidig, hvis tumorerne er asymptomatiske, anbefales det at overvåge dem, det vil sige regelmæssigt at udføre MR-scanning, for ikke at gå glip af begyndelsen på deres forstørrelse.
Ordinationen af et bestemt lægemiddel bestemmes af patientens type tumor.
Farmakoterapi af tumorer, der udskiller PRL, udføres med lægemidler fra gruppen af stimulatorer af dopamin D2-receptorer i hypothalamus (selektive dopaminagonister), og de mest anvendte er Bromocriptin (Parlodel, Bromergol), Norprolac og ergotderivatet Cabergolin eller Dostinex til hypofysemikroadenom med øget prolaktinsekretion.
Bivirkninger af Dostinex (Cabergolin) kan omfatte allergiske reaktioner; hovedpine og svimmelhed; kvalme, opkastning og mavesmerter; forstoppelse; en følelse af svaghed eller træthed; søvnforstyrrelser. Og blandt bivirkningerne af Bromocriptin (ud over allergiske reaktioner) er brystsmerter; øget puls og vejrtrækning med en følelse af åndenød; hoste blod op; forringet koordination af bevægelser osv.
Lægemidlerne Octreotid (Sandostatin), Lanreotid (Somatulin) og Pegvisomant, der anvendes mod mikro- og makroadenomer, der udskiller væksthormon, er hæmmere af STH og antagonister af dets receptorer.
Og til ACTH-secernerende neoplasmer i adenohypofysen med Itsenko-Cushing syndrom anvendes Metyrapone (Metopirone) eller Mitotane (Lysodren).
Kirurgisk behandling bør overvejes for velfungerende (hormonelt aktive) mikroadenomer. I tilfælde, hvor konservativ behandling er ineffektiv, og tumoren har en let suprasellær ekspansion i sella turcica, kan hypofyseadenomektomi ordineres - en operation for at fjerne hypofysemikroadenomet. I øjeblikket udføres transnasal eller transsfenoidal mikrodissektion, det vil sige fjernelse af hypofysemikroadenomet gennem næsen.
Mulige komplikationer og konsekvenser af fjernelse af hypofyse-mikroadenom omfatter postoperativ blødning og lækage af cerebrospinalvæske (som ofte kræver reoperation), samt betændelse i meninges, synshandicap, hæmatomdannelse, forbigående diabetes insipidus og recidiv af mikroadenomet.
Homøopati til behandling af hypofyse-mikroadenom med hyperprolaktinæmi bruger lægemidler, hvis virkning kan bidrage til delvist at lindre symptomerne. For eksempel ordineres et middel fremstillet af blæksprutteblæk Sepia og et middel fremstillet af eng-kolibriumplanten Pulsatilla til uregelmæssig menstruation og amenoré, og til galaktoré ordineres et middel baseret på roden af europæisk alpeviol.
Man bør naturligvis ikke håbe, at folkebehandling af hypofyse-mikroadenom kan være mere effektiv. Og ikke kun fordi herbalister med denne diagnose kun lader sig lede af patienternes klager (uden at kende deres sande ætiologi), men også på grund af upålideligheden af mange "folkemediciner". Man behøver ikke at gå langt for at finde eksempler.
Nogle internetkilder anbefaler at bruge en blanding af primula, ingefærrod og sesamfrø for at reducere prolaktinniveauet. Men primula hjælper med langvarig tør hoste, udtynding af slim, og ingefærrod udviser, ligesom sesamfrø, laktogene egenskaber.
Du kan også finde råd om at tage en tinktur af slyngel. Men i virkeligheden bruges dette middel indvortes mod luft i maven og udvortes mod gigtsmerter i led. Slyngel blev højst sandsynligt forvekslet med rødderne af sort cohosh (andre navne for det er sort cohosh og sort cohosh), som bruges mod hedeture i overgangsalderen.
Ernæring til hypofyse-mikroadenom bør være afbalanceret - med reduceret sukker- og saltindtag. Dette er ikke en særlig diæt, men blot en kaloriefattig diæt.
Alkohol er udelukket i tilfælde af hypofyse-mikroadenom.
Hvilken læge skal jeg se ved et hypofyse-mikroadenom? Endokrinologer, gynækologer og neurokirurger beskæftiger sig med de problemer, der opstår med denne type tumor.
Forebyggelse
Fordi de miljømæssige eller livsstilsmæssige årsager til hypofysetumorer er ukendte, er der simpelthen ingen måde at forhindre udviklingen af hypofysemikroadenomer.
Vejrudsigt
De fleste hypofysetumorer kan kureres. Hvis et hormonelt aktivt hypofysemikroadenom diagnosticeres i tide, er chancerne for helbredelse høje, og prognosen er gunstig.
Handicap og hypofysemikroadenom: Handicap kan være forbundet med tumorvækst og skade på synsnerven, samt andre konsekvenser af denne patologi, hvis sværhedsgrad er individuel. Og anerkendelse af en patient som handicappet afhænger af eksisterende helbredsproblemer og niveauet af funktionelle forstyrrelser, som skal opfylde lovgivningsmæssigt godkendte kriterier.
Mikroadenom i hypofysen og hæren: Patienter med denne tumor (selv hvis den er fjernet) bør ikke overophede, opholde sig i solen i lang tid og overanstrenge sig fysisk. De er derfor ikke egnede til militærtjeneste.
Hvor længe lever man med hypofyse-mikroadenom? Denne tumor er ikke kræft, så der er ingen grænser for den forventede levealder. Selvom patienter med aktivt STH-producerende mikroadenom kan udvikle hypertension og en forøgelse af hjertestørrelsen, og dette kan reducere deres forventede levealder betydeligt. En øget risiko for død hos patienter over 45 år ses ved Itsenko-Cushings sygdom og akromegali.

